12 月 12 日,麻省理工学院旗下分拆公司 Tome Biosciences(以下简称“Tome”)正式走出隐匿模式,并宣布完成 A 轮融资。该轮融资总额达 2.13 亿美元,包括 Arch Venture Partners、Polaris Partners、Andreessen Horowitz 和 GV 等多家投资机构为其事业添砖加瓦。
Tome 公司方声称,其资金将用于开发一种新的基因编辑技术,即“可编程基因组整合(PGI)”技术。该技术旨在将不同长度的遗传物质高效地插入基因组中,而不会损坏或破坏 DNA。该公司相信,这种基因编辑技术能够克服现有方法的一些局限性。

实际上,早在两年前 Tome 成立之时,该公司及其技术就已经成为了基因编辑领域中一个“公开的秘密”。该公司的两位联合创始人 Omar Abudayyeh 和 Jonathan Gootenberg 曾在博德研究所跟随 CRISPR 先驱张锋开展研究,之后来到麻省理工学院麦戈文脑研究所工作。2022 年,两人共同发表了 PGI 技术相关论文。
“我们的技术能够将任意大小、任意位置的基因序列插入到任意基因组中。” Tome 公司方对此总结道。目前,该公司尚未披露任何管线进展和适应症信息。
01
“粘贴”基因,最长可插入 5 万碱基对
Tome 所采用的方法可以追溯到 2021 年所发布的一篇预印本论文,该论文于 2022 年发布于 Nature Biotechnology 期刊。

(来源:Nature Biotechnology)
论文中介绍了一种名为 PASTE(Programmable Addition via Site-specific Targeting Elements)的新型基因编辑工具,其在 CRISPR 基础上开发,并且能够以更安全、更有效的方式替换突变基因,可向哺乳动物及人类细胞中定点插入长达 36,000 个碱基的 DNA 长片段。
作为一种可编程整合系统,PASTE 结合了 CRISPR 的靶向方法,以及丝氨酸整合酶所带来的高效插入优势。
最开始,研究团队关注到丝氨酸整合酶能够将包含 attP 附着位点的序列插入到含相关 attB 附着位点的靶点中,其插入序列最长可达 5 万个碱基对。
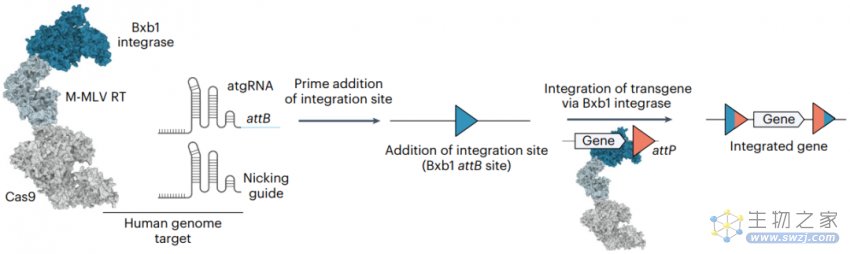
▲图丨 PASTE 基因编辑示意图(来源:Nature Biotechnology)
然而,想要直接使用这些整合酶也存在很大挑战,因为其在基因组上的附着位点十分固定,很难将其进行重编程以定位到其他位点。
对此,研究团队提出,将 CRISPR-Cas9 的靶向能力与整合酶结合,有望实现大片段基因插入。
基于这一思路,PASTE 工具中使用 Cas9 切口酶切割特定的基因组位点。在此过程中,Cas9 切口酶融合的逆转录酶将整合酶所需的附着位点序列整合进切割位点,从而可以将整合酶所需的附着位点插入基因组中的任何位置。并且这种方法仅需切断 DNA 一条链,不会引起 DNA 双链断裂。
“PASTE 的概念实际上非常简单,”研究的通讯作者之一、麻省理工学院麦戈文脑研究所研究员 Jonathan Gootenberg 对此介绍道,“这是一个两步过程,我们首先插入一小段恒定序列,这很容易做到,然后利用该常量序列塞入一段更大的序列。”
目前,Tome 所使用的 PGI 技术正是基于 PASTE 技术进一步发展而来。根据 Tome 网站公开信息来看,目前 PGI 技术能够插入的序列尺寸为 100 至 10,000 碱基对。
02
PASTE≈Prime?双方否认专利纷争
麻烦的是,PASTE 在设计方面与 Prime Medicine 旗下的 prime editor 存在一些相似性,这引起了相关业内人士的注意。因为后者也使用 Cas9 蛋白和逆转录酶,并且在某些情况下与整合酶配对。人们因此担心两者之间的知识产权可能会存在交叉。
但 Tome 公司方表示其并不担心专利方面的问题。该公司总裁兼首席执行官 Rahul Kakkar 坚称,Tome 手持来自于麻省理工学院授权的“非常可靠”的专利组合,目前已知的包括美国专利 11572556、11827881 和 11834658。
另一方面,知名华裔科学家、Prime Medicine 联合创始人 David Liu 也曾公开表明其观点,认为 PASTE 和 Prime 的 PASSIGE 方法之间存在差异,即 PASTE 是将 prime 编辑器和整合酶融合成一条蛋白质链,而 PASSIGE 仍然将其作为两个独立的蛋白质使用。
David Liu 同时评价道,“在人类细胞的几个不同靶点上,我们同时比较了融合或未融合的主编辑器和整合酶系统,但我们从未观察到融合主编辑器和整合酶有任何好处。”
无论如何,Tome 凭借高效、准确的长序列编辑技术赢得了业界内的普遍关注。因此,当基因编辑技术专家 John Finn 受邀担任该公司的首席科学官时,他表示“无法拒绝”。在此之前,Finn 曾是 Codiak Biosciences 的发现研究副总裁,以及 Intellia Therapeutics 的平台生物学和肝脏药物发现执行总监。
而该公司领导者 Rahul Kakkar 曾是自身免疫药物制造商 Pandion Therapeutics 的前首席执行官,该公司后来以 18.5 亿美元的价格被出售给默沙东。

▲图丨Rahul Kakkar(来源:Tome Biosciences)
管线方面,Tome 目前尚未披露任何候选药物以及目标适应症。据 Kakkar 表示,该公司的细胞治疗项目中涉及“一些非常大的适应症”,但也没有透露任何具体疾病,仅仅提到其希望在明年的科学会议上展示其进展。
不过,根据此前的一些宣传材料,Tome 早期曾表示将推动用于治疗肝脏疾病的基因疗法和治疗自身免疫性疾病的细胞疗法,并且希望在 2026 年开始进行人体测试。除此之外,一些单基因突变导致的罕见病也是 PGI 技术所擅长的领域。
参考资料:
1.https://tome.bio/
2.https://www.globenewswire.com/news-release/2023/12/12/2794660/0/en/Tome-Biosciences-Launches-with-Over-200-Million-in-Funding-to-Advance-Programmable-Genomic-Integration-Platform.html
3.https://doi.org/10.1038/s41587-022-01527-4