近年来,人类多能干细胞(hPSC)和诱导多能干细胞(iPSC)被广泛用于各种组织和器官的定向分化研究。这类研究在再生医学、细胞治疗和构建人类复杂疾病模型等领域具有广泛的前景。其中,由hPSC定向分化而来的胰岛B细胞(SC-β-cell)已经证明可以分泌胰岛素,从而调节血糖水平【1-7】。这项技术可以用于治疗因胰岛B细胞缺失导致的1型糖尿病,目前已进入一期临床试验阶段【8】。然而,目前的定向分化方法并不能精确地控制细胞分化方向,导致分化终产物中包含了一种分泌血清素的内分泌细胞。这种细胞被视为定向分化过程的副产物。此外,体外分化得到的胰岛B细胞在功能上与人类胚胎期的B细胞相似,处于未完全成熟的状态。这些不成熟的B细胞在胰岛素分泌水平和细胞内葡萄糖代谢方式上与完全成熟的B细胞有所差异。这些问题都严重影响了SC-β-cell在未来细胞治疗工程中的有效性和安全性【9】。造成这些问题的原因之一是因为目前研究人员对于人类胰岛B细胞的发育和成熟过程还没有完全了解,尤其是在这一过程中的基因表达调控尚未被全面揭示。
2023年4月10日,加州大学圣地亚哥分校Maike Sander团队在Developmental Cell杂志发表题为Understanding cell fate acquisition in stem-cell-derived pancreatic islets using single-cell multiome-inferred regulomes的研究论文。这项研究采用单细胞组学、基因调控网络构建和基因编辑技术,全面揭示了体外培养中的SC-β-cell基因表达调控,并与成熟人类胰岛B细胞进行比较,解析了体外培养条件下缺失的B细胞成熟信号。

研究人员收集了SC-β-cell在体外培养过程中不同阶段的细胞,以及从儿童和成年人体内提取的原代胰岛细胞。然后,他们进行了单细胞基因表达和染色质开放性分析,通过关联转录因子、非编码的顺式作用元件和下游的目标基因,构建了胰岛B细胞发育与成熟阶段的基因调控网络。此外,研究人员还结合之前发表的人类胚胎胰腺发育的单细胞基因表达图谱,与他们构建的基因调控网络进行整合分析。他们发现在人类胚胎期,胰腺中存在一种短暂的分泌血清素的B细胞,这种细胞与在体外培养过程中出现的“副产品”B细胞非常相似。这两种细胞中血清素的产生都受到转录因子CDX2的调控,不同的是在胚胎发育过程中,B细胞逐渐失去CDX2和血清素分泌的能力,而在体外培养中的血清素分泌细胞虽然逐渐减少,但不会完全消失。研究人员进一步用CRISPR/Cas9在hPSC中敲除了CDX2基因 (CDX2-KO),将其分化至SC-β-cell。结果表明,缺少CDX2会导致体外分化过程中血清素分泌细胞产生的比例减少。此外,通过比较基因调控网络的方式,研究人员发现从儿童体内分离的胰岛B细胞中,多个信号通路下游的基因调控网络处于激活状态,这表明胰岛B细胞的成熟受到多个信号通路的调节。然而,在体外培养过程中缺少这些与B细胞成熟相关的信号,可能是导致体外培养的SC-β-cell不完全成熟的原因之一。在这些信号中,研究人员发现了雄性激素可以促进胰岛B细胞增殖。他们在体外培养的SC-β-cell中进行了实验证实了这一预测。
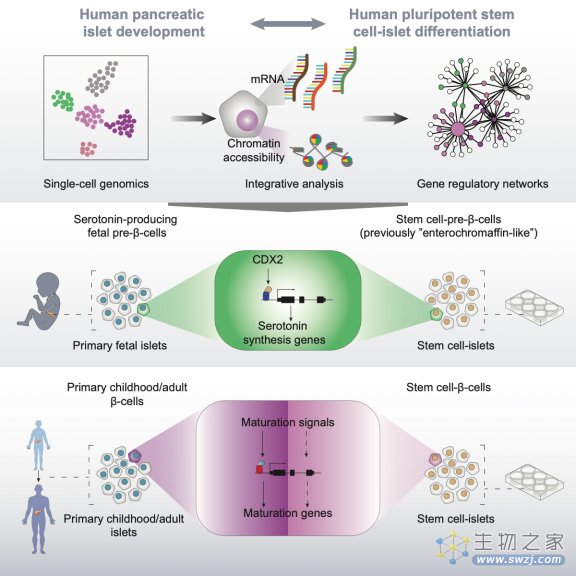
图1. 单细胞组学揭示hPSC定向分化为胰岛B细胞过程中的基因表达调控。注:Stem cell-pre-β-cell代表体外培育过程中产生的分泌血清素的“副产品”B细胞。由于在之前的研究中被认为与肠系膜色素细胞类似,固又被称作“enterochromaffin-like” cells。
综上所属,这项研究系统性地描述了hPSC定向发育为胰岛B细胞的过程中的基因表达调控,同时通过与人类胚胎,儿童及成人胰岛细胞的比较,为今后精准调控B细胞体外发育提供了理论支持。
加州大学圣地亚哥分校博士后研究员朱晗博士和王高伟博士为本文共同第一作者,Maike Sander教授为本文通讯作者。目前,王高伟博士已入职南京大学现代生物研究院展开独立研究工作,欢迎感兴趣的同学加入。
原文链接:
https://doi.org/10.1016/j.devcel.2023.03.011
参考文献
1. Rezania, A., Bruin, J.E., Riedel, M.J., Mojibian, M., Asadi, A., Xu, J., Gauvin, R., Narayan, K., Karanu, F., O'Neil, J.J., et al. (2012). Maturation of human embryonic stem cell-derived pancreatic progenitors into functional islets capable of treating pre-existing diabetes in mice. Diabetes 61, 2016-2029. 10.2337/db11-1711.
2. Pagliuca, F.W., Millman, J.R., Gürtler, M., Segel, M., Van Dervort, A., Ryu, J.H., Peterson, Q.P., Greiner, D., and Melton, D.A. (2014). Generation of functional human pancreatic β cells in vitro. Cell 159, 428-439. 10.1016/j.cell.2014.09.040.
3. Nostro, M.C., Sarangi, F., Yang, C., Holland, A., Elefanty, A.G., Stanley, E.G., Greiner, D.L., and Keller, G. (2015). Efficient generation of NKX6-1+ pancreatic progenitors from multiple human pluripotent stem cell lines. Stem Cell Reports 4, 591-604. 10.1016/j.stemcr.2015.02.017.
4. Velazco-Cruz, L., Song, J., Maxwell, K.G., Goedegebuure, M.M., Augsornworawat, P., Hogrebe, N.J., and Millman, J.R. (2019). Acquisition of Dynamic Function in Human Stem Cell-Derived β Cells. Stem Cell Reports 12, 351-365. 10.1016/j.stemcr.2018.12.012.
5. Nair, G.G., Liu, J.S., Russ, H.A., Tran, S., Saxton, M.S., Chen, R., Juang, C., Li, M.L., Nguyen, V.Q., Giacometti, S., et al. (2019). Recapitulating endocrine cell clustering in culture promotes maturation of human stem-cell-derived β cells. Nat Cell Biol 21, 263-274. 10.1038/s41556-018-0271-4.
6. Hogrebe, N.J., Augsornworawat, P., Maxwell, K.G., Velazco-Cruz, L., and Millman, J.R. (2020). Targeting the cytoskeleton to direct pancreatic differentiation of human pluripotent stem cells. Nat Biotechnol 38, 460-470. 10.1038/s41587-020-0430-6.
7. Balboa, D., Barsby, T., Lithovius, V., Saarimäki-Vire, J., Omar-Hmeadi, M., Dyachok, O., Montaser, H., Lund, P.E., Yang, M., Ibrahim, H., et al. (2022). Functional, metabolic and transcriptional maturation of human pancreatic islets derived from stem cells. Nat Biotechnol. 10.1038/s41587-022-01219-z.
8. Ramzy, A., Thompson, D.M., Ward-Hartstonge, K.A., Ivison, S., Cook, L., Garcia, R.V., Loyal, J., Kim, P.T.W., Warnock, G.L., Levings, M.K., and Kieffer, T.J. (2021). Implanted pluripotent stem-cell-derived pancreatic endoderm cells secrete glucose-responsive C-peptide in patients with type 1 diabetes. Cell Stem Cell 28, 2047-2061.e2045. 10.1016/j.stem.2021.10.003.
9. Nguyen-Ngoc, K.V., Wortham, M., and Sander, M. (2022). Sizing up beta cells made from stem cells. Nat Biotechnol 40, 1006-1008. 10.1038/s41587-022-01271-9.