据不完全统计,目前,国内已32款AAV基因治疗药物IND申报获批,其中,3款进入III期临床。按照其IND获批时间顺序汇总如下:

1、九天生物的SKG0201
近日,九天生物(Skyline Therapeutics)在研的AAV基因治疗药物SKG0201注射液IND获国家药监局批准,开展治疗I型脊髓性肌萎缩症(SMA)的I期临床试验。

SKG0201注射液是一款用于单次静脉注射给药治疗I型SMA的新一代SMN1基因替代治疗药物,创新设计的载体由独特的中枢神经(CNS)特异性启动子调控、密码子全面优化的人源SMN1 cDNA构成。这一创新设计可实现更好的组织靶向性,使正常的SMN1基因导入体内后在中枢神经区域实现最大治疗效果、在低剂量下即可快速恢复正常的SMN蛋白在运动神经元中的表达,从而更安全有效地改善运动神经元等受累细胞的功能。针对SMA的明确致病机理和现有药物在安全性等方面存在的局限性,SKG0201这款全面创新设计的SMN1基因替代治疗药物,在其临床前研究中即展示了优越的疗效和安全性。SKG0201注射液在一项由上海交通大学医学院附属新华医院开展的治疗I型SMA的研究者发起的临床研究中,已完成了多个剂量组受试者入组,并在连续的随访评估中显示了良好的耐受性和治疗效果。
2、方拓生物的FT-002
2023年11月6日,方拓生物科技(苏州)有限公司(简称“方拓生物”)自主研发的创新型基因治疗药物FT-002注射液获CDE临床试验许可,拟治疗由RPGR(Retinitis Pigmentosa GTPase Regulator)基因变异导致的 X连锁视网膜色素变性(XLRP)患者。

FT-002注射液是一款重组腺相关病毒(rAAV)载体基因治疗药物,利用rAAV携带目的基因,经眼内注射,使视网膜细胞可以表达有活性的RPGR蛋白,参与光感受器纤毛运输功能,挽救由于RPGR基因变异所导致的光感受器细胞缺失并改善患者的视功能或者延缓视力损伤进展。FT-002注射液IIT研究初步结果令人振奋,给药后患者黄斑区视网膜厚度、视野及视敏度等客观指标有明显改善,个别患者术后两个月观察到最佳矫正视力(BCVA)较基线期提高明显提高(ETDRS视力表)。
3、鼎新基因的RRG001
2023年11月6日,上海鼎新基因科技有限公司(简称“鼎新基因”)宣布:由其自主研发生产的RRG001眼内注射液的临床试验申请(IND)已获CDE批准。RRG001眼内注射液是鼎新基因首款适用于年龄相关性湿性黄斑病变(nAMD)的基因治疗药物。

RRG001眼内注射液是鼎新基因拥有自主知识产权的重组腺相关病毒(rAAV)基因治疗药物,通过视网膜下腔给药将表皮生长因子受体(VEGFR)融合蛋白基因导入nAMD患者眼底,让眼底细胞成为蛋白工厂,不断表达患者需要的VEGFR融合蛋白,避免了传统抗体频繁给药的弊端,以期达到“一次给药、长期有效”的治疗黄斑病变效果。该药物已于2023年2月在江苏省人民医院开展了研究者发起的临床试验(IIT研究),初步的临床研究数据显示:受试者临床获益显著,且无任何严重不良事件发生。
4、九天生物的SKG0106
2023年10月,九天生物(Skyline Therapeutics)申报的AAV眼科基因疗法SKG0106获国家药监局批准临床,适应症为新生血管性年龄相关性黄斑变性(nAMD),此外,SKG0106已于今年6月获FDA批准开展治疗nAMD的全球I/IIa期临床试验。

SKG0106是一款在研创新眼科基因治疗药物,该疗法以重组AAV为载体表达独特的抗血管內皮生长因子(VEGF)蛋白,给药方式为玻璃体腔注射,具有一次给药长期有效的潜力。
5、诺洁贝生物的诺洁贝生物
2023年9月,苏州诺洁贝生物技术有限公司的AAV疗法NGGT001获国家药监局批准临床,NGGT001是由诺洁贝生物研发的一款治疗结晶样视网膜变性(BCD)的创新性基因治疗药物。
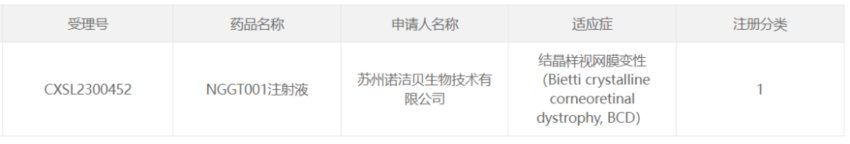
NGGT001是一款基于rAAV2载体的在研基因疗法,通过表达密码子优化的CYP4V2来治疗BCD。在野生型小鼠和Cyp4v3敲除小鼠模型中,视网膜下单次注射NGGT001,在眼室内实现了CYP4V2蛋白的稳定载体转导和长期表达;在成年食蟹猴视网膜下注射单剂量NGGT001,视网膜和脉络膜组织中观察到稳健的载体分布和持续的CYP4V2 mRNA表达,且在13周的毒理学研究中,显示这一疗法通过视网膜下给药耐受性良好。
6、杨森(Janssen)的JNJ-81201887
2023年8月初,强生(Johnson & Johnson)旗下杨森(Janssen)申报的AAV基因疗法JNJ-81201887(AAVCAGsCD59)获CDE临床试验默示许可,拟开发用于治疗继发于年龄相关性黄斑变性的地图样萎缩成人患者。

JNJ-81201887(JNJ-1887,AAVCAGsCD59)是一种基于AAV载体的在研基因疗法,旨在增加可溶性CD59(sCD59)的表达,保护视网膜细胞,从而减缓和预防疾病进展。
7、信致医药的BBM-H803
2023年7月24日,信念医药公司(Belief BioMed,BBM)全资子公司上海信致医药科技有限公司和上海勉亦生物科技有限公司申报的“BBM-H803注射液”临床试验申请获临床试验默示许可,适应症为血友病A。

BBM-H803是信念医药拥有自主知识产权的AAV基因治疗药物,通过静脉给药将人凝血因子Ⅷ基因导入血友病A患者体内,从而提高并长期维持患者体内凝血因子水平。
8、天泽云泰的VGM-R02b
2023年7月13日,上海天泽云泰生物医药有限公司(简称“天泽云泰”)自主研发的VGM-R02b获得国家药品监督管理局批准同意开展治疗戊二酸血症I型的临床试验。
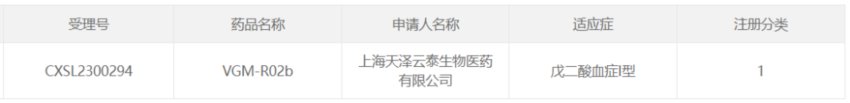
VGM-R02b是一种防止婴幼儿及儿童期戊二酸血症造成严重或危及生命的疾病进展的潜在治疗方法,也是全球首个用于戊二酸血症I型(GA-I)的基因治疗产品,该疗法基于基因替代原理,以重组腺相关病毒(rAAV)为载体,该疗法于2022年5月25日获得FDA授予其用于治疗GA-I的罕见儿科疾病认定(RPDD)资格。
9、 方拓生物的FT-004
2023年7月12日,方拓生物研发的针对血友病B(内源性FIX活性≤2%)的AAV基因治疗药物FT-004获得CDE临床试验许可。
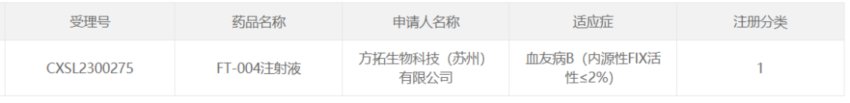
FT-004是一款基于AAV载体的基因治疗药物,临床前数据表明,FT-004可高效进入肝脏细胞,可持续、稳定表达及分泌功能性hFIX蛋白至血液中,能够长期有效地提高模型动物的凝血能力,且安全性良好。
10、 至善唯新的ZS802
2023年6月28日,四川至善唯新生物科技有限公司(以下简称“至善唯新”)针对血友病A的AAV基因治疗药物“ZS802注射液”获CDE批准,即将开展临床I/II期试验。

ZS802是至善唯新自主研发的AAV基因治疗药物,采用公司自主开发的全球最小肝脏特异性启动子,解决了被包装基因容量大的难题,显著提高了产品质量,此外,ZS802采用了至善唯新优化改造的FVIII基因序列,有效提高了其药效。目前,ZS802项目已在中国医学科学院血液病医院展IIT研究,其研究结果初步证明了该药物的安全性和有效性。
11、 嘉因生物的EXG102-031
2023年6月1日,杭州嘉因生物科技有限公司(以下简称“嘉因生物”)的AAV基因治疗药物EXG102-031眼用注射液获CDE批准,适应症为:湿性年龄相关性黄斑变性( wAMD)。
该疗法以AAV为载体过表达一种治疗性融合蛋白,能够结合/中和所有已知的血管内皮生长因子(VEGF)和血管生成素-2(ANG2)亚型,理论上一次给药长期有效。
12、安龙生物的AL-001
2023年4月27日,北京安龙生物医药有限公司(以下简称“安龙生物”)宣布,公司的眼科基因治疗产品“AL-001眼用注射液”IND已获CDE批准,适应症为:湿性年龄相关性黄斑变性(wAMD)。2023年5月29日,安龙生物发布消息称,该项目获得了研究组长单位北京协和医院机构项目立项和伦理委员会的批准,标志本项目正式进入了临床试验阶段。
该疗法是国内针对wAMD获批的首款通过脉络膜上腔(SCS)注射给药的基因疗法,该疗法以AAV为载体过表达抗VEGF蛋白,理论上一次给药长期有效。该产品采用了先进的、自研的无弹状病毒Sf9悬浮细胞rAAV生产工艺。
13、方拓生物的FT-003
2023年4月26日,方拓生物宣布FT-003注射液的临床试验申请(IND)获CDE临床试验许可,该产品适应症为新生血管性年龄相关性黄斑变性(nAMD)。
FT-003注射液是一种新型重组腺相关病毒基因治疗药物。临床前研究数据显示,FT-003注射后可高效感染动物视网膜多层细胞,使其持续表达和分泌抗血管生成因子,降低血管内皮通透性,抑制新生血管的生成。患者一次注射,期望获得长期疗效。
此外,FT-003治疗糖尿病黄斑水肿(Diabetic Macular Edema,DME)IND申请也已获CDE临床试验许可。

2023年05月19日,天津医科大学眼科医院李筱荣教授团队顺利完成了FT-003治疗DME国内首例患者给药。
14、辉大基因的HG004
2023年4月18日,辉大(上海)生物科技有限公司(简称“辉大基因”)宣布,公司自主研发的首个眼科AAV基因治疗药物HG004的IND已获CDE批准,适应症为:2型Leber's先天性黑蒙(LCA2),此外,今年1月,HG004已获得FDA的IND许可。

HG004是一款AAV介导的基因替代疗法,旨在治疗RPE65基因突变相关性视网膜病变,RPE65基因突变可能会导致严重的早发性儿童视网膜营养不良、早发性严重视网膜营养不良、Leber先天性黑蒙(LCA)或视网膜色素变性(RP)等。HG004采用的AAV载体针对视网膜色素上皮的转导率相比AAV2至少提高10倍,起始有效剂量远低于已上市的AAV2-hRPE65(LUXTURNA)。HG004在中国上海新华医院开展的IIT临床研究中,取得了良好的临床疗效,患者的视力得到了明显实质性的恢复。
15、纽福斯的NFS-02
2023年4月14日,纽福斯生物科技有限公司的AAV基因治疗药物NFS-02眼用注射液IND申请获CDE默示许可,适应症为Leber遗传性视神经病变(G3460A)。此外,去年,NFS-02已获FDA的新药临床试验(IND)许可。

NFS-02是一款基于AAV2的新型眼内注射基因治疗药物,治疗基因可通过药物的单次玻璃体内注射被递送至患者受损的视神经节细胞,修复患者因基因突变而受损的线粒体生物呼吸链,进而使视神经节细胞恢复视功能。
16、华毅乐健的GS1191-0445
2023年1月16日,苏州华毅乐健生物科技有限公司的AAV基因治疗药物GS1191-0445注射液,用于治疗A型血友病的临床试验申请获CDE批准。
华毅乐健在2022年11月向CDE正式提交了该疗法IND申请并获得受理,成为国内进入IND阶段的血友病A治疗药物。此外,该药物在天津血研所开展了IIT研究,已入组了9例患者,用药后取得了良好的安全性和令人振奋的有效性数据。
17、朗昇生物的LX102
2022年12月23日,朗信生物宣布旗下朗信启昇(苏州)生物制药有限公司(朗昇生物)的AAV基因疗法产品LX102注射液的IND申请已获CDE批准,用于治疗湿性老年性黄斑变性(wAMD)。

该疗法是基于AAV载体的体内基因疗法,可将表达抗VEGF融合蛋白的目的基因导入患者视网膜细胞,理论上一次给药长期有效。在之前开展的IIT临床研究中,该疗法表现出良好的安全性与有效性。
18、锦篮基因的GC301
2022年12月20日,北京锦篮基因科技有限公司(锦篮基因)的AAV基因治疗药物GC301腺相关病毒注射液IND申请获CDE默示许可,适应症为早发型庞贝病(IOPD)。2023年6月2日,GC301在中国医学科学院北京协和医院顺利召开Ⅰ/Ⅱ期临床试验启动会,标志着GC301注射液用于治疗婴儿型庞贝病的临床试验在主研究中心正式启动。
其治疗策略为:一次性静脉输注给药后,治疗基因可全身广泛表达,以期补偿肝脏、肌肉、中枢神经系统等组织的GAA酶基因缺陷。GC301在研究者发起的临床研究(IIT)中表现出了良好的安全性与有效性。
19、中因科技的ZVS101e
2022年12月6日,北京中因科技有限公司(简称“中因科技”)的“ZVS101e注射液”IND申请获CDE默示许可,适应症为结晶样视网膜变性(携带CYP4V2双等位基因突变)。2023年2月20日,ZVS101e注射液I/II期临床试验在天津医科大学眼科医院顺利完成首例受试者入组给药。

ZVS101e是以AAV8为载体的基因替代疗法,其针对适应症与治疗原理与2022年11月获批临床试验的天泽云泰的VGR-R01一致。
20、锦篮基因的GC304
2022年11月,北京锦篮基因科技有限公司(锦篮基因)的AAV基因治疗药物GC304腺相关病毒注射液(“GC304注射液”)IND申请获CDE默示许可,用于高甘油三酯血症伴复发性急性胰腺炎患者的治疗用药。
GC304基因药物装载的治疗基因为脂蛋白脂酶 (LPL)基因,LPL是水解血浆脂蛋白中甘油三酯 (TG)的关键酶。
21、弘基生物的KH631
2022年11月15日,康弘药业子公司成都弘基生物科技有限公司(弘基生物)的AAV基因治疗药物“KH631眼用注射液”5项IND申请获得国家药监局默示许可,用于治疗新生血管性(湿性)年龄相关性黄斑变性(wetAMD)。2023年5月初,首都医科大学附属北京同仁医院魏文斌教授团队完成了KH631治疗AMD的I期临床试验首例患者给药。
根据公司公开的相关专利信息,KH631通过AAV过表达VEGF拮抗剂达到治疗效果。(全文链接:康弘药业AAV基因疗法获批5项临床)
22、天泽云泰的VGR-R01
2022年11月1日,上海天泽云泰生物医药有限公司(天泽云泰)的AAV基因治疗药物VGR-R01注射剂IND申请获得CDE默示许可,其适应症为CYP4V2基因突变导致的结晶样视网膜变性(Bietti crystalline dystrophy, BCD)(全文链接:天泽云泰BCD基因治疗药物IND获批)。

23、锦篮基因的GC101
2022年10月,北京锦篮基因科技有限公司研发的AAV基因治疗药物GC101腺相关病毒注射液(“GC101注射液”)获得CDE临床试验默示许可,临床适应症为1型脊髓性肌萎缩症(1型SMA),同年11月15日,“GC101注射液”针对2型SMA适应症的IND申请获CDE默示许可。
24、方拓生物的FT-001
2022年9月,方拓生物针对RPE65双等位基因变异遗传性视网膜变性的基因治疗药物FT-001注射液的临床试验申请(IND)获CDE默示许可。2023年01月09日,方拓生物宣布,FT-001注射液在北京协和医院完成首例患者给药(全文链接:方拓生物FT-001注射液完成首例患者给药)。

25、至善唯新的ZS801
2022年9月1日,四川至善唯新生物科技有限公司的ZS801注射液临床申请获CDE批准,用于18岁及以上男性重度、中重度B型血友病(先天性凝血因子IX缺乏症,凝血因子IX<2%)患者出血的控制和预防。
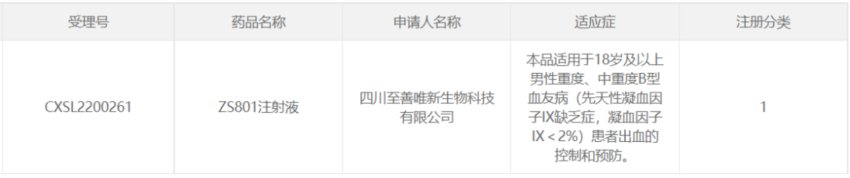
这是一款AAV基因疗法,此疗法采用的AAV载体的血清型在患者中预存的中和抗体非常低,可覆盖更多的中国患者。
26、嘉因生物的EXG001-307
2022年6月21日,嘉因生物宣布其自主研发的AAV基因疗法EXG001-307注射液的临床试验申请获得CDE批准,用于治疗1型脊髓性肌萎缩症(1型SMA),伴有存活运动神经元1(SMN1)基因的双等位基因突变(缺失)。

这是中国境内首个被批准进入注册临床试验的静脉注射治疗1型SMA的基因治疗产品(全文链接:国内又一款AAV基因疗法IND临床试验获CDE批准)。EXG001-307是一款以AAV为载体的基因疗法,有望一次给药长期有效,其作用原理及其用法,与诺华的Zolgensma相似。杭州嘉因针对EXG001-307采用了创新的设计,目的在于降低对心脏和肝脏的副作用,利于更好发挥其治疗效果。
27、天泽云泰的VGB-R04
2022年4月,上海天泽云泰生物自主研发的首个AAV基因疗法候选药物VGB-R04注射液获临床试验许可,用于治疗先天性凝血因子IX缺乏引起的血友病B。
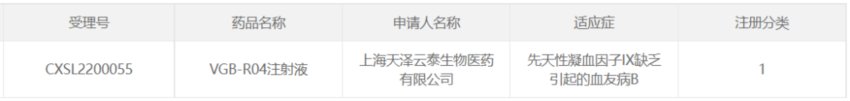
VGB-R04以静脉注射方式给药,通过AAV衣壳介导目的基因(治疗基因)递送至肝脏细胞核,在肝脏细胞中表达凝血因子Ⅸ变体(hFIX Padua)蛋白,FIX-Padua 是一种天然存在的具有高度活性的 FIX 变体 (R338L),其活性约为普通野生型FIX 的8 倍,意味着可以在更低的表达水平完成正常凝血功能,这样就降低了病毒载体的给药剂量,提高了病毒载体给药的安全性和药效。
28、朗昇生物的LX101
2022年4月,朗信生物旗下上海朗信启昇(朗昇生物)生物制药有限公司自主研发的AAV2-RPE65基因治疗制剂LX101眼用注射液获临床试验许可,用于治疗RPE65双等位基因突变相关的遗传性视网膜变性(IRD)患者。
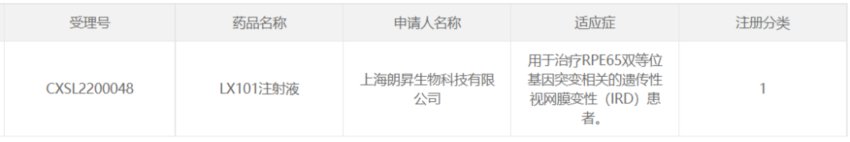
基因疗法LX101以AAV2为载体,将正常功能的且编码序列经优化的RPE65基因,导入体内视网膜细胞,补偿因该基因突变导致的蛋白功能缺失,恢复视力。在此前进行的研究者发起的临床研究中,该基因疗法表现出良好的安全性和有效性。
29、诺华的OAV101(已进入III期临床)
2022年1月,诺华(Novartis,NYSE:NVS)在中国递交的SMA基因治疗药物OAV101注射液(Zolgensma)临床试验申请获得临床试验许可。2022年4月29日,相关数据库显示,该疗法首次在国内启动临床试验,拟在中国入组20人,该临床试验属于全球3期临床STEER研究的中国部分。2022年6月20日下午,诺华(Novartis)基因疗法(OAV101)临床试验中国研究中心启动会在组长单位北京大学第一医院顺利召开,该临床试验属于全球III期临床STEER研究的中国部分,由北京大学第一医院儿科熊晖教授牵头,面向2~18岁初治2型脊髓性肌萎缩症(简称SMA)患者。

Zolgensma是一种治疗1型SMA的基因替代疗法,理论上一次给药长期甚至终生有效,是从本质上治疗此疾病的一次性治疗方案。此基因疗法用scAAV9载体经静脉输注将正常SMN1基因导入患者体内,产生正常的SMN1蛋白,从而改善运动神经元等受累细胞的功能。相比之下,治疗SMA的药物Spinraza和Evrysdi则需要长期重复给药,Spinraza每四个月通过脊柱注射给药一次,而Evrysdi是一种需每日口服药物。
30、信致医药的BBM-H901(已进入III期临床)
2021年8月,信念医药全资子公司上海信致医药科技有限公司自主研发的用于B型血友病治疗的基因疗法药物BBM-H901注射液获临床试验许可,2021年12月底,临床试验顺利完成首例受试者给药,目前已进入临床III期,预计在2024年下半年到2025年上半年上市销售。

BBM-H901是一款静脉给药AAV的基因疗法,AAV搭载的目的基因(治疗基因)可过表达人凝血因子IX(hFIX),从而提高并长期维持患者体内凝血因子水平,适用于预防血友病B成年男性患者出血。BBM-H901是国内最早开展临床试验的AAV基因治疗药物之一,从2019年就开始IIT临床研究(NCT04135300),IIT临床研究结果显示此疗法具有良好的安全性和有效性,给药后,受试者体内凝血因子IX(hFIX)水平显著提高,血液中hFIX水平长期稳定,患者年化出血率显著降低,且无明显的不良反应出现。
31、纽福斯的NR082(已进入III期临床)
2021年3月,纽福斯的NR082眼用注射液获得国家药品监督管理局颁发的注册性药物临床试验(IND)许可。2021年6月28日,纽福斯宣布,中国首个临床阶段的眼科体内AAV基因治疗药物NR082的I/II/III期第一阶段临床试验在中国完成首例患者入组及给药。2023年2月22日,纽福斯宣布,NR082眼用注射液用于治疗ND4突变引起的Leber遗传性视神经病变的III期临床试验在中国完成全部患者入组给药。

NR082基因治疗药物以AAV作为载体,用于ND4线粒体基因突变引起的Leber遗传性视神经病变(LHON),给药方式为单次玻璃体内注射,将治疗性基因通过玻璃体腔注射递送至患者受损的视神经节细胞,修复线粒体生物呼吸链,使视神经节细胞恢复活力与视功能。
32、舒泰神的STSG-0002(试验及后续开发已终止)
2019年6月中旬,乙肝AAV基因疗法STSG-0002由舒泰神(北京)生物制药股份有限公司申请临床试验,2019年9月中旬获得国家药品监督管理局批准针对慢性乙肝治疗的临床试验。2020年8月,完成首例受试者给药。

STSG-0002是一种以AAV为载体的基于RNA干扰技术的DNA基因治疗药物,由舒泰神研发,相对于非病毒载体的小核酸RNA药物,该药物药效时间明显更长,有望一次给药长期有效。