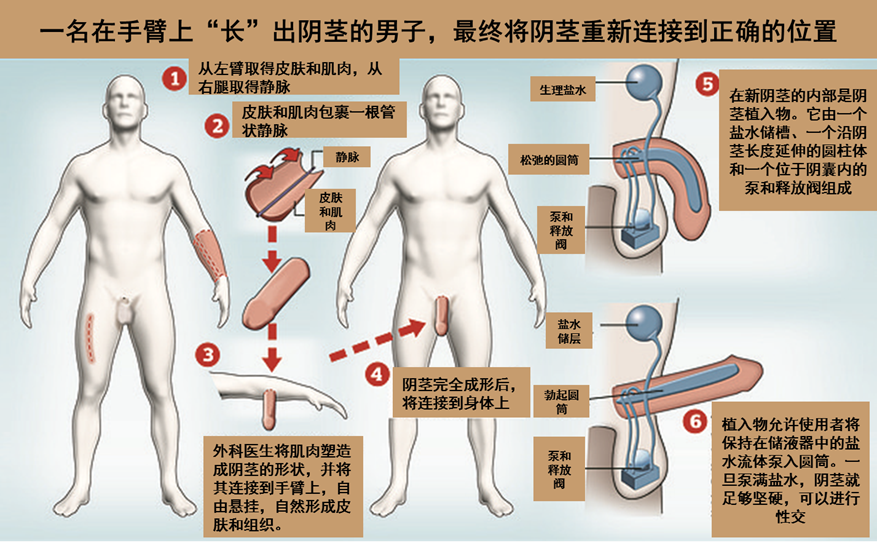
近年来,结直肠癌是癌症早筛企业关注的热点领域。目前,FDA批准的结直肠癌早筛产品有Exact Sciences的Cologuard(PMA编号:P130017),以及Epigenetics的Epi proColon(PMA编号:P130001)。Guardant Health也在最新的财报中透露今年已向FDA提交申请资料。
无论是按照发生率排序还是按照死亡率排序,结直肠癌都常年位居癌症前三。根据美国癌症协会预估,2022年一整年将新增151,030名结直肠癌病例,52,580名死亡病例。此外,早期结直肠癌的五年生存率可高达91%,远超出中晚期结直肠癌的五年生存率。对风险人群进行早期筛查具有长远的卫生健康意义,故而也给开发厂商带来了巨大的市场和利润空间。
因此长期以来,结直肠癌早筛一直是各大厂商的兵家必争之地。特别是当Exact Science的Cologuard从拿到FDA PMA证后商业上获得了巨大的成功之后,Guardant Health和Freenome紧随其后,推出了同类产品。
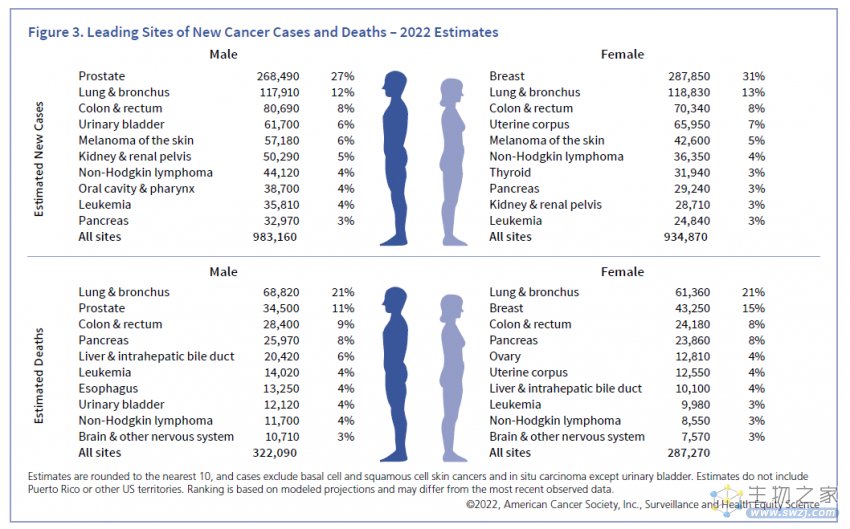
出自美国癌症协会American Cancer Society
而在一众“挑战者”里,Freenome当属其中翘楚,深受投资者青睐。该公司在过去的8轮融资中总共筹集到了11亿美元,最近的一次融资发生在今年1月11日,由罗氏投资了2.9亿美元。罗氏诊断首席执行官Thomas Schinecker对于该轮投资表示:“我们相信基于血液的多模式筛查和由数据驱动的医学见解将有助于提供个性化的医疗保健。这项投资将是推进早期癌症筛查的重要一步,我们期待在这一旅程中加入Freenome。”

罗氏诊断首席执行官Thomas Schinecker
技术方面,根据官网透露, Freenome采用蛋白组学+转录组学+基因组学+其他组学的多组学平台对于血液样本进行分析,再使用机器学习方式来进行癌症的早期检测。结直肠癌早筛测试是Freenome目前正在开发的第一个血液测试,该测试正在通过PREEMPT CRC进行临床验证。
上文提到的PREEMPT CRC是一项前瞻性、针对平均风险参与者的大型多中心研究,在城市和农村社区200多个研究地点展开,包括社区医院、卫生系统、私人诊所、三级医疗中心和教学医院,共招募了40,000多名受试者。该试验本身建立在先前另一项前瞻性、多中心的AI-EMERGE研究之上,AI-EMERGE研究表明Freenome平台检测结直肠癌的灵敏度为91%,特异度为91%。
Freenome作为结直肠癌早筛的后起之秀,其对于该领域的认识自然值得关注和借鉴。因此,医疗媒体公司MEDTECH DIVE特别与Freenome首席执行官Mike Nolan展开了一场对话,针对其产品和战略等问题进行了详细讨论。
以下为对话内容:

Freenome首席执行官Mike Nolan
MEDTECH DIVE:进入2023年,你的重点是什么?
Mike Nolan:结直肠癌早筛的血液检测测试将是我们多组学平台提供的第一个产品。这对于我们来说是非常重要的一步。
我们目前结束了结直肠癌研究的招募,共有40,000多名受试者完成了注册。这意味着我们将有40,000多名受试者的血液样本、结直肠镜检查报告和组织病理学报告。现在我们在进行这些后续步骤以继续推进我们的工作,从而将产品带到临床护理的第一线中。
MEDTECH DIVE:你打算将产品提交至FDA申请注册么?
Mike Nolan:是的,我们将申请该产品FDA的注册,这对于我们来说很重要。我们希望测试不仅是可用的,而且还易于获得。
FDA的批准对我们会有所帮助,因为批准会让我们的产品能够更好地被指南所纳入,特别是美国PSTF(Preventive Services Task Force)指南。产品被纳入这些指南后,我们能够更好地向患者提供它,同时价格方面不会让许多人无法承受。
MEDTECH DIVE:为什么专注于血液而非粪便样本?
Mike Nolan:当你观察那些被诊断出患有结直肠癌的人时,你会发现他们并没有经常做肠镜,但这些人往往一直进行抽血检查。
抽血员通常放两根管子就可以完成抽血。但如果是采集粪便样本,我必须自己动手收集粪便,采样,打包并送往实验室。这一系列过程会造成样本破损。
MEDTECH DIVE:你是如何设计临床试验的?
Mike Nolan:我们在临床试验过程中发现,需要我们真正深入当地社区才能了解临床试验是如何运作的。我们从一开始就致力于尽我们所能来解决与健康公平和可得性相关的一些问题。
在我们的临床试验过程中,我们一直反问自己:如何才能进入社区,真正地去理解“信任”这个概念?比如说,你住在某个邮政编码区,你会为了参加临床研究而专门前往另一个邮政编码区么?并且,要参与研究的话你必须做肠镜,这已经让很多人感到不安。现在他们还要见一个不认识的消化科医生,这些都让临床研究的后勤工作变得更加复杂。当所有这些事情开始堆叠起来后,他们真正参与临床试验的可能性降低了。因此,我们通过与社区领袖合作来了解正在发生的这些事情。
MEDTECH DIVE:你遇到的一些反馈是什么?
Mike Nolan:有些人认为这些检测只适合男性,有些认为它只适合女性,还有些人认为这个检测不是真实存在的。有些人担心自己被对待的方式:会收到额外的支付账单么?他们在动态参与过程中会不会有其他问题?
我们通过了解这一点,现在拥有了此类研究中最具临床多样性、社会经济多样性和地理多样性的研究。因为我们会自己看美国人口普查数据,并努力将我们的受试人群具有整个美国人口的代表性。因此,当我们去寻找FDA的时候,我们的数据不是一个同质化的数据。
MEDTECH DIVE:你如何确保患者可以广泛获得这些测试,以及为什么价格很重要?
Mike Nolan:美国联邦医保医补中心(CMS)表示如果结直肠癌血液检测产品有74%的灵敏度和90%的特异度,那么就可以得到全国范围的覆盖。当下事态就是这么紧急,如果CMS真的伸出了援手,这对于美国结直肠癌患者来说无疑是一个强烈支持的信号。
如果你从非侵入性的粪便测试中得到阳性结果,然后再去做诊断性肠镜检查,那么就有几百美元的经济要求一直阻碍患者参与其中。这足以造成整个结直肠癌的标准护理过程的中断。但是现在有个强大的推动力来让这一切都成为可能,几百美元的经济要求阻碍正在消失。
除此之外,还有一件事,就是我在Freenome的五年工作时间里,结直肠癌平均风险年龄已经从50岁下降到45岁。这也是一个真正的驱动力,我们看到结直肠癌的发病时间越来越早,对于人们的影响也越来越大。
目前在美国有950万例还未进行的肠镜检查。
MEDTECH DIVE:是什么导致了这些积压?
Mike Nolan:在新冠大流行期间,由于人们担心在手术过程中被感染新冠,因此不愿意去进行肠镜检查,造成了检查的推迟和积压。现在更重要的是,我们需要真的走出来通过任何手段去发现潜在的癌症,无论是通过粪便检测,或是肠镜检查,还是血液检测。
MEDTECH DIVE:在新冠大流行之前,有多少人进行了结直肠癌筛查?
Mike Nolan:美国癌症协会曾在几年前表示:“到2018年之前,要让80%有资格接受结直肠癌筛查的人群接受筛查”。但即使在2018年以后,也就是刚刚进入新冠大流行的时候,我们得到最接近的数据是67%,这还是在平均风险年龄降低之前的数据。
MEDTECH DIVE:你预期你们测试费用是多少?
Mike Nolan:现在粪便检测费用大约是500美元。我们认为我们也会差不多同样的价格范围,大约500美元,但我们的观点是绝大多数病人将不必支付任何费用,这是因为第三方支付机构、政府支付机构、政策制定者和领导人都在真正地介入,做了很多工作来帮助人们在没有经济负担的情况下获得这种服务。
MEDTECH DIVE:如何应对竞争?多种检测的市场空间有多大?
Mike Nolan:我们的真正竞争对手是癌症,我们有动力去真的战胜癌症。然后我们也鼓励这个领域中的其他竞争对手去做一些不同的事情,不要只是和别人做同样的事情。我们要围绕癌症从不同的角度、维度出发。
打个比方,我们就像一个搜索队——我们应该分散开来进行搜索,而不是一群人聚集着排成一列去搜索。每个人都在做他们自己的事情,这会比较好。因为从患者可及性和依从性方面出发,对一个患者有用的东西,对另一个患者就不一定有用。
如今,包括结直肠癌早筛在内的癌症早筛早已成为美国IVD领域的热点。但这一赛道内群雄逐鹿,目前虽然已经有头部企业如Exact Sciences、Guardant Health等,但最终鹿死谁手犹未可知。
国内IVD企业如果能够抓住这一机会,推动癌症早筛产品出海,所能获得的长远收益,甚至有可能胜过新冠检测。
未来,HMC还将持续关注美国结直肠癌早筛的动态,想要了解更多信息,可以订阅我们的HMC欧美市场和临床Club,或者联系我们的分析师进行咨询。