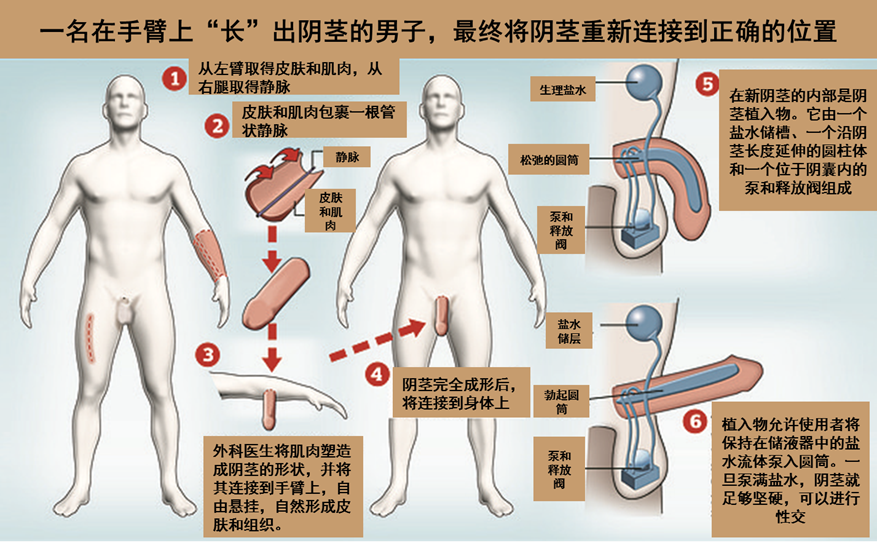
8年前,2014年,王义丹在华东师范大学入学。她在细胞里“编程”。她没想到,为了同一个研究课题,从硕士研究生到博士研究生,到博士后三年级,持续努力了8年,她终于设计出首个人工合成的抗病毒系统,并成功进行了测试。投稿就投了两年,论文终获发表。
近日,相关论文在线发表在国际知名期刊《自然·通讯》(Nature Communications)上。王义丹该是论文的第一作者。上述抗病毒系统的名字ALICE(爱丽丝)与电影《生化危机》中的女主角同名。她说,该系统成功模拟了人体的抗病毒免疫系统。
但既然人体本来就有抗病毒免疫系统,为什么还要人工合成一个?
该论文称,在面对病毒性疾病时,免疫系统受损病患的并发症和死亡风险更大。而且,开发广谱抗病毒药物是防范大流行病的重要措施。
上述论文的通讯作者是华东师范大学叶海峰研究员和杜克-新加坡国立大学医学院教授、美国微生物科学院院士、澳大利亚技术科学与工程院院士王林发。
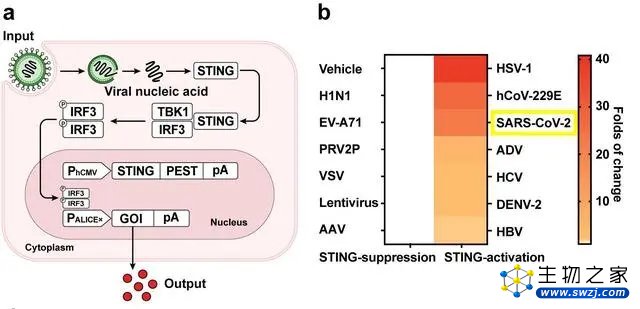
ALICEsen系统的原理设计图(a),以及该系统对新冠病毒(SARS-CoV-2)等13种病毒的反应(b)。12月15日,叶海峰告诉澎湃科技(www.thepaper.cn),ALICE系统可以被认为新型的广谱抗病毒的智能活体“药物”,或智能化的机器人一样的人造免疫系统。它能够自动的监测、感应,病毒来了,它能自动被激活,输出抗病毒蛋白,把病毒清除掉。它是“二合一”甚至“三合一”的加强版的免疫系统,综合了人体细胞和细菌中的抗病毒“武器”;更重要的是,它是智能的闭环设计,有病毒时就启动清除,没病毒时就“沉默”,“没人这么集成过”。它含有病毒传感器、多重抗病毒输出模块等模块,可以灵活调整,迭代更新。
加强版、多重抗病毒系统:闭环更智能
“病毒那么小,为什么危害那么大?”
王义丹说,上大学时,她就对病毒学研究特别感兴趣,读研时本来想考中国科学院武汉病毒研究所,但未能如愿,她随后在华东师范大学攻读硕士研究生学位。导师叶海峰在了解到她的研究兴趣后,开始建议、指导、支持她做人工合成抗病毒系统的课题。“叶老师的想法很超前,那时候还是2014年。”
在常规的对抗病毒过程中,人体免疫系统在发现病毒后,会产生干扰素等“武器”,抑制或清除病毒。但这样的过程需要数天甚至一两周的时间才能完成。有时候远水解不了近渴。
此外,在临床治疗中,或防疫过程中,人们常常是先检测到病毒,再针对性地服用药物,或设计疫苗,存在一定的滞后性和局限性。
最新发表的ALICE系统,把发现病毒的“病毒传感器”和对抗病毒的多重“武器”整合在一起,一“检测”到病毒,就启动清除程序,反应时间缩短,在数小时内就开始响应。并且,该系统根据病毒的剂量进行响应,病毒多时,产生的抗病毒蛋白就多;病毒被清除后,系统“静默”。
叶海峰表示,这样的抗病毒系统是闭环的,自反馈和自调控,更加“自动、智能”。

示意图:研究团队用“后羿射日”的典故比拟ALICE系统的作用原理。装载有ALICE基因线路的底盘细胞被比作后羿,其武器箭矢是不同类别的抗病毒功能蛋白。后羿精准操控弓箭,击碎病毒。水凝胶包裹的细胞移植实验显示,在小鼠体内,无论在病毒感染发生的前、中、后期,ALICE系统均能自动感知和抑制病毒。尤其值得注意的是,ALICE系统携带的中和抗体输出模块,可在病毒感染后的六小时自动输出,比人体适应性免疫系统产生中和抗体至少提早了一周。
论文显示,ALICE系统含有多重抗病毒的功能模块:人源的抗病毒细胞因子干扰素IFN-α和IFN-β的基因、来自细菌的可降解病毒核酸的Cas9蛋白的基因、以及人源的分泌型中和抗体的基因。
该系统的“病毒传感器”是人体细胞中“天然”存在的接头蛋白STING蛋白。该蛋白在细胞中“遭遇”病毒核酸时,将信号传递到细胞信号网络中。
ALICE系统可以通过两种方式被递送到实验对象体内:一种是基因治疗方式,利用基因治疗载体进行递送;另一种是细胞治疗方式,将上述系统重编程在细胞中,再把细胞移植到实验对象体内。
由腺相关病毒(AAV)载体递送ALICE系统至疱疹性角膜炎(HSK)小鼠模型的眼角膜实验结果显示,实验小鼠角膜、三叉神经节以及大脑中的病毒载量得到抑制;并且面对病毒的迭代感染,也能发挥良好的抗病毒效果。
研究人员介绍,针对疱疹病毒HSV-1导致的疱疹性角膜炎,目前,临床上治疗HSV-1的常用方法是抗病毒药物,如阿昔洛韦(ACV)等核苷类似物,这类药物靶点单一,极易造成耐药毒株的出现。而ALICE系统的出现,提供了一种灵活、创新、模块化的抗病毒治疗新策略。
投稿两年:测试了13种病毒,包括新冠病毒
王义丹告诉澎湃新闻,虽然她对病毒学研究很感兴趣,但对人工合成抗病毒系统的研究,“当时真的是要放弃了,不想做了”。“(开始研究的)前两年我们连在病毒培养方面都有很大的困难。”
王义丹说,硕博连读期间,导师叶海峰给了她科研上最大的自由度和包容性,在自己感兴趣的领域自由探索外,也建议她同步开展了其他课题,才让她的博士研究生学位论文答辩顺利通过。
今年是她在叶海峰研究员课题做博士后的第三年,即将出站。
而论文投稿过程也一波三折。
2020年,他们第一次投稿。“审了两轮,补实验补了两次,改文章改了两轮,审稿人最后还‘反水’了,认为我们的系统还是没法在临床上解决问题,例如新冠肺炎的临床问题。”叶海峰透露。他表示,该论文的核心贡献之一是理念上的突破。传统做病毒学研究,可能没想过用合成生物学的思想,把病毒的传感器与治疗输出模块集成,形成一个闭环的传感器系统,相当于一个人造的免疫传感系统。“这种思想,这种概念,我觉得是最创新的。”目前的实验结果表明了应用的潜力,但很难仅仅通过一篇论文,就能够直接解决临床问题。
随后他们转投到《自然·通讯》期刊。直到2022年12月9日论文正式在线发表,整个投稿过程长达2年时间。
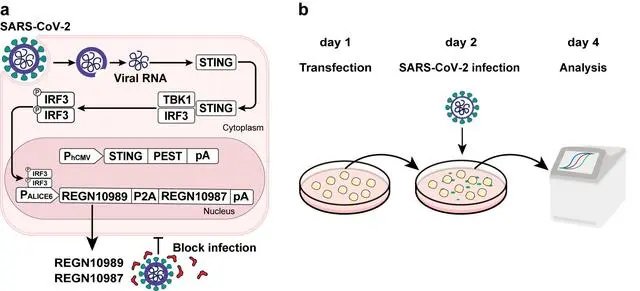
细胞实验显示,ALICE系统可识别新冠病毒,并降低其拷贝数。王义丹介绍,论文中,他们一共测试了5种细胞系,还测试了登革热病毒(DENV-2)、乙肝病毒等13种病毒,其中包括新冠病毒(SARS-CoV-2)。
论文显示,新冠病毒也能激活ALICE系统。HEK-293T细胞实验结果显示,与对照组相比,转染了含中和抗体REGN10989和REGN10987的ALICE系统的细胞中,其新冠病毒的载量低了70.3%(±4.3%)。未来可以用最新发现的中和抗体来升级ALICE系统。
叶海峰表示,但上述关于新冠病毒的实验只是细胞实验,尚未进行临床试验。其临床应用,还需要进一步研究。上述新冠病毒的细胞实验是在合作单位中国科学院武汉病毒研究所的P4实验室(生物安全四级实验室)中进行。
叶海峰表示,“我们是有数据的,这个系统是能够识别新冠(病毒),新冠病毒是能够激活ALICE系统。”
他表示,在临床应用的概念设计中,以抗新冠为例,因为新冠病毒主要还是感染呼吸道,通过基因治疗的方法,把ALICE系统喷入鼻腔,从而进入其表皮细胞。当呼吸到新冠病毒时,鼻腔表皮细胞中的ALICE系统被激活,快速输出中和抗体,阻止新冠病毒后续的进一步感染。

著名病毒学家、华东师范大学校友、杜克-新加坡国立大学医学院教授、美国微生物科学院院士、澳大利亚技术科学与工程院院士王林发。华东师范大学生命科学学院 提供在细胞里编程的人:“站在全人类的角度看待问题”
“他跟我说,你一定要站在全人类的角度看待问题。他这句话,一直都激励着我。”
“做科研就是这样,你要实实在在的解决问题。”
王义丹特别提及的这两句话,来自著名病毒学家、华东师范大学校友、杜克-新加坡国立大学医学院教授、美国微生物科学院院士、澳大利亚技术科学与工程院院士王林发。2018年,他回华东师范大学做讲座,并开始对王义丹关于ALICE系统的研究给予指导。
叶海峰表示,“原本我们只想着用Cas9核酸酶把病毒的核酸降解掉,王林发老师就给我们一个建议,说你可以试试中和抗体,快速表达一个蛋白,直接中和也更好。后面我们又做了既输出Cas9,又输出中和抗体,然后后面我们还又做了输出干扰素的,思路就打开了。”

华东师范大学叶海峰研究员叶海峰表示,现在看起来简单得像堆积木一样,但其实ALICE系统研究的每一步都不容易。“一个细胞因子到底怎么表达?效率高不高?能不能分泌出来?(抗病毒)效果好不好?这些都要试。但最难的,我觉得是传感器本身,如果这个传感器不work,或者效果很差,没有后面的应用价值的,几乎不会有效果。这里耽搁了蛮长时间。”
王义丹认为,ALICE系统目前最接近临床应用的,可能是针对HSV-1病毒导致的疱疹性角膜炎。因为疱疹病毒会潜伏感染,目前常规的病毒药物难以彻底清除病毒,但如果把ALICE系统制成滴眼液,滴在眼角膜上,可以实现抗病毒的“潜伏”部署。
叶海峰表示,做出像细胞机器人一样的智能化活体药物,“这是我的目标。”最好是能够口服的,吃下去之后能够自动监测生理状态,当生理状态不好了,根据基因线路算法,细胞机器人能够输出药物。
叶海峰提到,除了临床应用,他目前已经接到关于兽药研发方面的咨询,比如关于非洲猪瘟、禽流感等动物疾病。
而据澎湃新闻此前报道,叶海峰课题组2017年报告了远红光调控的转基因表达控制系统,实现智能手机远程控制细胞释放胰岛素来治疗糖尿病的目标;2018年,报告了远红光调控的CRISPR-dCas9内源基因转录激活装置(FACE),可实现表观遗传操控以及诱导干细胞分化为功能性神经细胞;2020年,报告了远红光调控的分割型split-Cas9基因编辑系统(FAST),可对小鼠肿瘤中的致癌基因进行编辑;2022年初,报道了新一代超灵敏光遗传学工具(REDMAP),只要红光照射1分钟,实现糖尿病小鼠降血糖。
叶海峰表示,核心要义是人工设计,通过设计,人工构建基因线路、基因开关、生物传感器,最终达成目标。
王义丹说,“可以这样理解,我们是在细胞里面做编程,在细胞里面去编辑各种元件,让它们程序化地来执行功能。”“在电脑上设计好,然后再把它们合成出来,在细胞里面进行测试。”
她说,研究ALICE系统的八年里,她也担心过论文被其他人抢发,所以每天都要查合成生物学领域最新发表的“线路”、元件和设计,并加快实验。
未来还敢迎接这样的挑战吗?
王义丹说,“我觉得肯定没问题,一方面坚持自己喜欢的课题,另外其他有实际应用价值的课题也要做。”